Définition
Dosage : Mesure de la concentration d’une solution.
Etalonnage : mesures précises de concentrations connues de l’EC à doser que l’on comparera avec celle de notre échantillon de concentration inconnue.
Autres cours à consulter
Le dosage par étalonnage expliqué en vidéo
La vidéo s’appuie sur les notes de cours développées ci-dessous.
Source – chaine Youtube : « phychiers »
Protocole pour TOUS les dosages par étalonnage
- Préparer, par dilution, plusieurs solutions étalons de concentrations connues (on gagne en précision) : ce sera notre gamme d’étalonnage.
- Mesurer une grandeur physique (en seconde la masse volumique (ρ), en spécialité l’absorbance A ou la conductivité (σ) ) pour chacune des solutions étalons
- Tracer un graphique : A = f (C) ou ρ = f (C) ou σ = f (C)
- Mesurer la grandeur physique (A, 𝜎 ou 𝜌) de la solution à doser puis reporter sur le graphique pour déterminer sa concentration.
Dosage à l'aide de la masse volumique (seconde)
Mesure de la masse volumique des solutions étalons
On mesure la masse volumique de quelques solutions étalons (=solutions de concentrations connues).
Tracer du graphique : ρ = f(C)
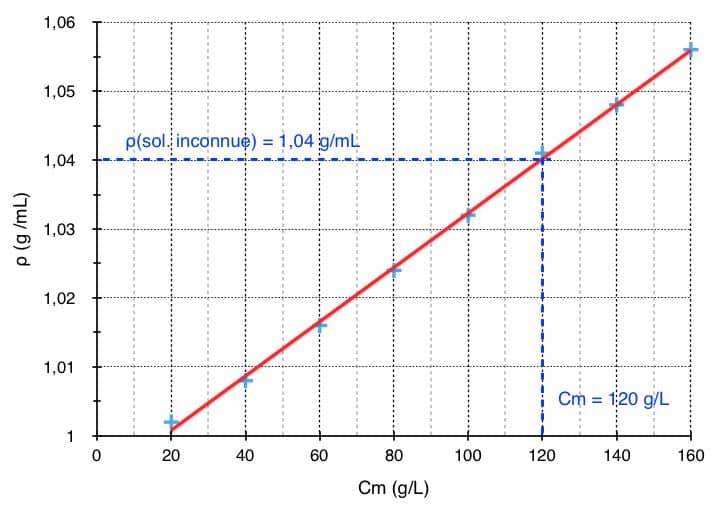
- Les croix bleues ciels correspondent aux mesures de masse volumique et concentrations des solutions étalons.
- Les pointillés bleus correspondent à la construction graphique qui permet de faire correspondre la mesure de masse volumique de la solution inconnue avec sa concentration.
Dans le cas où ρ (sol. inconnue) = 1,04 g/mL alors la droite d’étalonnage nous indique : Cm = 120 g/L
Dosage spectrophotométrique (première)
Mesure de l'absorbance des solutions étalons
Toutes les mesures d’absorbance A ci-dessous ont été réalisées à l’aide d’un spectrophotomètre à la longueur d’onde d’intensité maximale λmax.
Tracé du graphique : A = f (C)
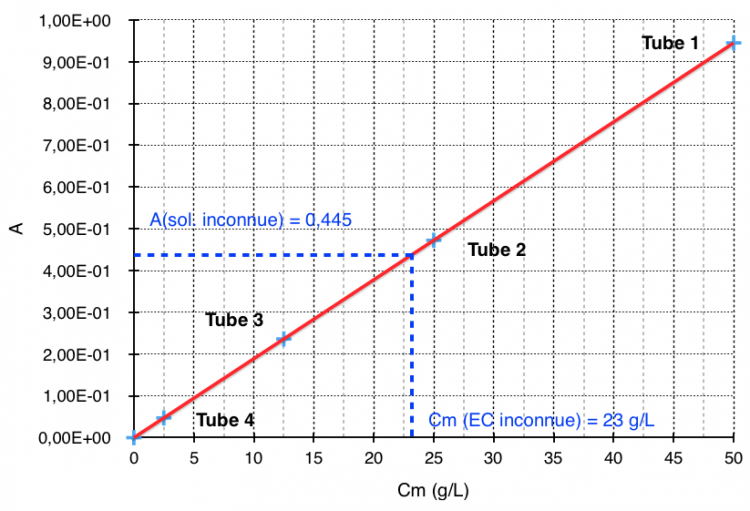
- Les croix bleues ciels correspondent aux mesures d’absorbance des tubes 1, 2, 3, et 4.
- Les pointillés bleus correspondent à la construction graphique qui permet de faire correspondre la mesure d’absorbance de la solution inconnue avec sa concentration.
Dans le cas où A (sol. inconnue) = 0,445 alors la droite d’étalonnage en ions cuivre II nous indique : Cm = 23 g/L
Dosage par étalonnage conductimétrique (terminale)
Dosage conductimétrique (& titrage conductimétrique)
Vous simulerez un TP qui cherche à déterminer la concentration en chlorure de sodium d’un sérum physiologique. Vous pourrez :
- préparer la droite d’étalonnage pour doser par étalonnage une échelle de teinte
- ou simuler le dosage par titrage de la solution de concentration inconnu à l’aide d’une solution de nitrate d’argent.